Idrocarburos
Los Hidrocarburos son un grupo de compuestos orgánicos que contienen principalmente carbono e hidrógeno. Son los compuestos orgánicos más simples y pueden ser considerados como las substancias principales de las que se derivan todos los demás compuestos orgánicos.
Pueden encontrarse de forma líquida natural (petróleo), liquida por condensación (condensados y líquidos del gas natural), gaseoso (gas natural) y sólido (en forma de hielo como son los hidratos de metano).
La explotación del petróleo y del gas natural representa una industria muy importante para la economía ya que permiten obtener combustibles fósiles y producir lubricantes, plásticos y otros productos.
Clasificación
Cabe resaltar que es posible clasificar los hidrocarburos como alifáticos o aromáticos. Los hidrocarburos alifáticos, por su parte, pueden dividirse en alcanos, alquenos y alquinos de acuerdo a las clases de uniones que vinculan a los átomos de carbono.
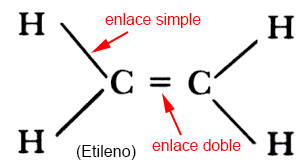
Los hidrocarburos alifáticos, según la teoría, son aquellos que carecen de anillo aromático. Pueden ser saturados o no saturados. Los saturados son los alcanos (grupo en el cual todos los carbonos poseen dos pares de enlaces simples), mientras que los no saturados (también conocidos con el nombre de insaturados) son los alquenos (que, como mínimo, presentan un enlace doble) y los alquinos (con enlaces triples).
Los hidrocarburos aromáticos, por su parte, son los compuestos que tienen, como mínimo, una estructura cíclica y que cumplen con lo que se conoce como la regla de Hückel.
La regla de Hückel
Con la regla de Hückel es posible estudiar la relación que tiene lugar entre la aromaticidad y la cantidad de electrones que se pasan de un átomo a otro cuando se solapan los orbitales sp2 de una molécula de tipo orgánico cíclico y plano que alterna enlaces simples y dobles. Cuando el número de estos electrones es 4 n + 2 se dice que la molécula es aromática, mientras que para 4 n, antiaromática. Un compuesto aromático presenta una estabilidad muy diversa a la de uno antiaromático o uno no aromático, por lo que para anticiparse a dicha propiedad esta regla es de vital utilidad.
Con respecto a los aromáticos, el benceno es el tipo de hidrocarburo más común. Se trata de una molécula en la cual es muy sencillo observar su nivel energético, de acuerdo a la presencia o ausencia de nodos. A través de la regla de Hückel, es posible tomar una cantidad n de orbitales de átomos y relacionarlos, partiendo del principio que establece que el resultado de dicho análisis es equivalente a la misma cuantía de orbitales pero con estados energéticos diversos.
Luego de aplicar dicha relación, en casos donde se tienen 4 n electrones, éstos alcanzan un nivel de energía relativamente más alto, mientras que cuando se encuentran 4 n + 2, fórmula que anteriormente se adjudicó a las moléculas aromáticas, los electrones pasan a un estado considerablemente menor y logran una mayor estabilidad.
sustancias basicas
SOLUCIONES ÁCIDAS Y BÁSICAS
En nuestra vida diaria tenemos continuos contactos con soluciones ácidas y básicas.Veamos ejemplos:
ACIDAS
SUSTANCIA – ÁCIDO PRESENTE – FÓRMULA
Cítricos – Ascórbico – C6 H8 O7
Vinagre – Acético – C2H4O2
Leche – Láctico – C3H6O3
Jugos – Clorhídrico – HCL
Baterías de autos – Sulfúrico – H2SO4
Las soluciones ácidas tienen sabor ácido (agrio).
Atacan a ciertos metales llamados activos.
Contienen hidrógeno
BASES
SUSTANCIA – BASE PRESENTE – FÓRMULA
Desodorantes – Hidróxido de aluminio – Al (OH)3
Yeso blanco – Hidróxido de calcio – Ca (OH)2
Soda caústica – Hidróxido de sodio – Na OH
Laxantes gástricos – Hidróxido de magnesio – Mg (OH)
Limpiadores – Hidróxido de amonio – NH4OH
Las soluciones básicas tienen sabor amargo.
Producen sensación jabonosa al tacto.
Todas contienen, salvo el amoniaco, hidrógeno, oxígeno, al menos un metal.
Sería temerario intentar descubrir la acidez o basicidad de una solución desconocida probando qué gusto o tacto tienen. Afortunadamente, existen sustancias que con su color nos indican la acidez o basicidad de una disolución. Se les denomina indicadores. (El azul bromotimol disuelto en alcohol es un indicador seguro.
Si a una base se le añade un ácido, ocurre un cambio químico llamado neutralización.
En la neutralización se destruyen las propiedades del ácido y de la base. Ello explica por qué se usa una base para contrarrestar el efecto de un ácido, y viceversa. Así, el escozor que producen las ortigas, que se debe a una sustancia ácida, se calma poniendo sobre la piel bicarbonato de sodio, y la picadura de abeja que lleva una sustancia básica, se calma con un poco de vinagre.webgrafía: www.google.com.co/sustanciasacidasybasicas/monografias Publicado por sustancias acidas y basicas en 11:36 No hay comentarios:

TIP PARA HACER EXPERIMENTOS CON SUSTANCIAS ACIDAS O BASICAS
Desde muy antiguo se sabe que pueden formarse dos grandes grupos de sustancias:
Uno que tiene propiedades ácidas y otro con propiedades básicas o alcalinas.La palabra ácido proviene del latín acetum que quiere decir vinagre.
Alcalino deriva de la palabra árabe alkali que significa ceniza.
Estas propiedades son opuestas y, cuando se mezclan sustancias ácidas con básicas, ambas se anulan entre sí, resultando de la mezcla nuevas sustancias que serán ácidas, básicas o neutras), dependiendo de la fuerza relativa de las sustancias de partida.
Vas a hacer una serie de experimentos que te permitirán comprobar qué sustancias o mezclas que utilizas corrientemente tienen propiedades ácidas y cuáles básicas.
Todos los recipientes o útiles que utilices deben estar perfectamente limpios y debes asegurarte de que al final de tu trabajo queden exactamente igual de limpios. No es concebible un buen trabajo de experimentación química sin mantener un riguroso orden y una escrupulosa limpieza.

El sitio donde trabajes debe ser de fácil limpieza, debes tener siempre a mano un trapo para recoger los líquidos que puedan derramarse.
Los ácidos y las bases producen distintas reacciones:
El color que tienen muchas flores, plantas o frutas es debido a que producen unas sustancias con la propiedad de estar coloreadas.
Precisamente, estas sustancias son capaces de cambiar su color si se encuentran en presencia de un ácido o una base. Por ello se llaman «indicadores», porque indican, mediante el cambio de color, si están en contacto con un ácido o una base.
Para tus experimentos sobre ácidos y bases utilizarás el color de las ciruelas negras, de la col lombarda o de frutos y bayas de color azul, morado o negro.
Los ácidos tienen un sabor agrio, colorean de rojo el tornasol (tinte rosa que se obtiene de determinados líquenes) y reaccionan con ciertos metales desprendiendo hidrógeno. Las bases tienen sabor amargo, colorean el tornasol de azul y tienen tacto jabonoso. Cuando se combina una disolución acuosa de un ácido con otra de una base, tiene lugar una reacción de neutralización. Esta reacción en la que, generalmente, se forman agua y sal, es muy rápida. Así, el ácido sulfúrico y el hidróxido de sodio NaOH.